Basic HTML Version
C
apitolo 12
j
Le basi molecolari dell’ereditarietà
31
Durante il processo di duplicazione, la stessa
DNA-poli-
merasi
corregge gli errori: quando trova un appaiamento di
basi sbagliato, rimuove la base errata procedendo a ritroso e
la sostituisce con quella corretta; quindi, riprende a scorrere
nella giusta direzione 5’
→
3’: per questo motivo, l’enzima è
chiamato
correttore di bozze
. Tale sistema di controllo per-
mette la riparazione di gran parte degli errori, la cui frequenza
complessiva si riduce a un nucleotide ogni miliardo di nucleo-
tidi copiati: la duplicazione si mantiene pertanto un processo
affidabile e rigoroso.
Nei danni indotti da agenti esterni come gli agenti chimici e
le radiazioni, la riparazione può consistere nell’asportazione del
tratto di DNA contenente il nucleotide sbagliato: si parla allora
di
excisione
. Poiché non sempre le mutazioni vengono ripa-
rate, con l’aumentare dell’età queste finiscono per accumularsi
aumentando così la probabilità che la cellula diventi cancerosa.
I meccanismi indicati consentono riparazioni a breve ter-
mine, dato che avvengono già pochi minuti dopo il danno. Se
però tali sistemi non funzionano, oppure se il danno è talmente
esteso da eccedere le loro capacità di riparazione, nei batteri
intervengono altri sistemi tra cui la cosiddetta
risposta SOS
:
si tratta di un sistema di allarme metabolico che aiuta la cel-
lula a “salvarsi” da condizioni potenzialmente letali, a scapito
dell’accuratezza della riparazione. Tali modalità di riparazione
sono talmente imprecise che normalmente risultano represse
e vengono attivate solo quando diventa più importante riem-
pire le lacune prive di acido nucleico piuttosto che controllare
la correttezza di ciò che è usato per riempirle.
Le mutazioni, per lo più dannose, raramente
possono rivelarsi un vantaggio
Una mutazione si inserisce in modo del tutto casuale in
un programma altamente organizzato che si è andato perfezio-
nando nel tempo: perciò, risulterà
per lo più dannosa, talvolta
innocua e solo molto raramente vantaggiosa
.
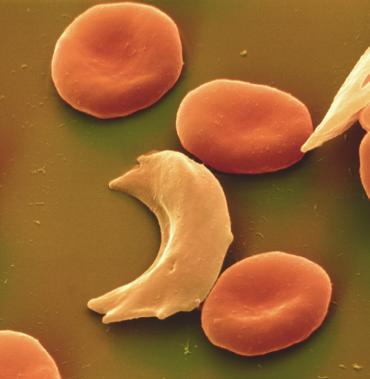
Consideriamo il caso della mutazione puntiforme a ca-
rico di un gene che codifica per l’emoglobina, e che è alla
base dell’
anemia falciforme
, malattia rara ma letale. In
alcune regioni dell’Africa centrale, dove prevale la foresta
pluviale e dunque l’ambiente ideale per la diffusione del-
la malaria, la frequenza dell’allele mutato
a
responsabile
dell’anemia assume valori particolarmente elevati, fino al
40%. Le conclusioni sono chiare: in un ambiente in cui la
malaria incide fortemente sulla mortalità della popolazione,
il genotipo eterozigote
Aa
deve rappresentare evidente-
mente un vantaggio selettivo. Il
vantaggio dell’eterozigo-
te
ha permesso, in questo caso, un netto incremento della
frequenza di un allele mutato, pur trattandosi di un allele
svantaggioso (
fig. 36
).
Anche un’altra malattia ereditaria caratterizzata dalla
forma anomala dei globuli rossi, la
talassemia
o
anemia
mediterranea
, è più frequente nelle aree storicamente più
colpite dalla malaria (oggi ormai bonificate): in Italia, alcune
fasce costiere toscane e laziali, il delta del Po, e poi Calabria,
Sicilia e Sardegna. Come per l’anemia falciforme, la mutazio-
ne all’origine della talassemia ha offerto il vantaggio di un
effetto “protettivo” nei confronti dell’infezione da plasmodio
della malaria.
Le stesse regioni mediterranee vedono una maggiore in-
cidenza del
favismo
, malattia ereditaria legata al cromosoma
X
, in cui si ha la carenza dell’enzima glucosio 6-fosfato deidro-
genasi contenuto nei globuli rossi. Tale condizione consente
una vita normale purché si eviti l’ingestione di alimenti come
le fave o l’assunzione di farmaci come i sulfamidici e l’acido
acetilsalicilico; altrimenti, si avrebbe l’inibizione di tale enzima,
già carente, e conseguente rottura delle membrane cellulari
dei globuli rossi e anemia grave (
tab. 1
).
Le mutazioni possono rivelarsi utili nella ricerca biome-
dica e genetica: basti pensare all’importanza dei mutanti di
Drosphila
utilizzati da Morgan (
fig. 37
a pagina precedente).
Fig.12.08 carta anemia
incidenza dell’anemia
falciforme
0-10%
10-20%
Zone malariche
Fig. 36
Il plasmodio
della malaria, un protozoo
veicolato dalla zanzara
Anopheles
, si riproduce
nei globuli rossi: l’altera-
zione dei globuli rossi nei
portatori eterozigoti di
anemia falciforme rende
questi ultimi più resistenti
alla malaria.
C12_006_049_EFG.indd 31
08/02/12 09.45

